Indice
La maculopatia essudativa (AMD essudativa) ossia la degenerazione maculare legata all’età di tipo neovascolare (Neovascolar Age- related Macular Degeneration, nAMD) è una grave patologia oculare che interessa la macula, ossia la porzione della retina centrale e responsabile della visione fine e dettagliata che ci permette di riconoscere un volto, leggere, eseguire lavori di precisione, guidare l’auto etc.
Nei Paesi tecnologicamente avanzati, l’incidenza dell’AMD è aumentata fortemente e continua ad aumentare a causa in primo luogo dell’incremento della vita media e della concomitanza di numerosi altri fattori ambientali e nutrizionali oltre a quelli genetici talora predominanti. L’AMD colpisce infatti circa l’11% delle persone di età compresa tra i 65 e i 74 anni e tale percentuale cresce sensibilmente man mano che si considerano fasce d’età più avanzata. Oggigiorno l’AMD rappresenta la causa più comune di cecità legale e di ipovisione nelle persone di età superiore ai 55 anni.
L’AMD può presentarsi in due forme: l’AMD atrofica (o non-neovascolare o secca) e l’AMD essudativa (o neovascolare o umida). L’AMD esordisce solitamente nella forma atrofica (90% dei casi) e più raramente (10% dei casi) nella forma essudativa. In alcuni pazienti l’AMD atrofica può evolvere in forma essudativa.
La maculopatia essudativa è causata dalla crescita incontrollata di neovasi patologici sotto la retina, un processo noto come neoangiogenesi patologica.
Il processo fisiologico “normale” (sano) che porta alla formazione di nuovi vasi sanguigni nel corpo (essenziale durante la crescita, la rimarginazione delle ferite o la gravidanza) è noto come angiogenesi; nel caso dell’AMD, però, i vasi sanguigni neoformati sono difettosi, malati, e per questo motivo si parla di neoangiogenesi patologica e di neovasi patologici.
Questi tendono a perdere sangue e fluidi sotto la retina e determinano il sollevamento della macula dalla sua posizione originale, causando così un danno all’epitelio pigmentato retinico (RPE) e ai fotorecettori che, se rimangono per molto tempo separati dalla loro fonte di ossigeno e nutrimento, vanno incontro a morte cellulare. La morte dei fotorecettori maculari determina la perdita della visione centrale, con la comparsa di una macchia scura o di un punto cieco al centro della visione. In presenza di emorragia al di sotto della macula si può avere la formazione di un tessuto cicatriziale che può portare alla perdita irreversibile della visione centrale in tempi relativamente brevi.
La neoangiogenesi patologica è causata da eventi fisiologici conseguenti al processo d’invecchiamento delle cellule e dei tessuti dell’occhio, quali la formazione di drusen confluenti, lo stress ossidativo e l’ipossia.
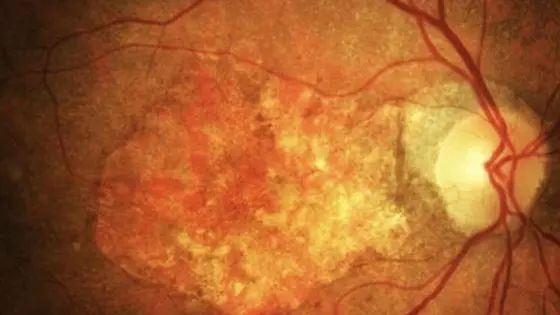
Le drusen sono minuscoli accumuli di materiale di scarto derivante dal metabolismo delle cellule retiniche, esse si formano sotto la retina – tra l’epitelio pigmentato retinico (RPE) e la Membrana di Bruch – e appaiono come delle piccole macchie di colore giallastro visibili all’esame del fondo oculare e alla retinografia. Nel tempo, le drusen tendono ad aumentare in numero e dimensioni fino a fondersi tra loro e formare ammassi di materiale di scarto più grandi noti come drusen confluenti.
Lo stress ossidativo è una condizione di grande disequilibrio delle cellule, che può determinare il malfunzionamento o la morte delle stesse. Lo stress ossidativo è causato dalla presenza di eccessive quantità di molecole altamente reattive, tra cui i radicali liberi. Molte di queste molecole si formano quotidianamente all’interno delle cellule come sottoprodotti del metabolismo o per azione dei raggi UV (fotossidazione) o entrano nelle cellule attraverso l’alimentazione (i radicali liberi sono abbondanti nei cibi cotti a temperature molto elevate). Solitamente, le specie reattive e i radicali liberi vengono neutralizzati o eliminati dalle cellule, ma con l’avanzare dell’età, alcune funzioni cellulari diventano meno efficienti e ciò può portare a una maggiore produzione e/o un minore smaltimento di queste molecole, che in questo modo si accumulano nelle cellule e nei tessuti. È molto importante sottolineare che la maggiore presenza di raggi UV nell’atmosfera – dovuta al buco dell’ozono – è una delle cause principali della formazione di radicali liberi a livello retinico, poiché anche i raggi UV arrivano direttamente sulla retina.
Per ipossia s’intende uno stato di scarso apporto di ossigeno a un tessuto. Nell’occhio, l’invecchiamento può portare ad un ispessimento della membrana di Bruch, che può diminuire o impedire il passaggio dell’ossigeno e dei nutrienti provenienti dai vasi sanguigni della coroide verso la macula. Allo stesso modo l’aumento di spessore della membrana di Bruch rappresenta un ostacolo alla rimozione dei cataboliti retinici. La presenza di drusen confluenti – caratteristiche dello stadio avanzato dell’AMD atrofica – causa un’ulteriore separazione della retina dallo strato vascolare e concorre quindi all’instaurarsi di una condizione d’ipossia.
La presenza di drusen confluenti, lo stress ossidativo e l’ipossia a livello della retina possono dar luogo a un processo d’infiammazione durante il quale vengono rilasciate particolari molecole denominate fattori di crescita endoteliali, che stimolano la formazione di nuovi vasi sanguigni. Il principale fattore di crescita identificato e coinvolto nell’insorgenza dell’AMD essudativa è il fattore di crescita dell’endotelio vascolare (VEGF), che si diffonde all’interno della coroide e stimola la crescita di nuovi vasi sanguigni patologici.
La formazione di neovasi patologici segna l’esordio della maculopatia essudativa. I neovasi patologici crescono dalla coroide e dalla coriocapillare, penetrano attraverso la membrana di Bruch e proliferano ulteriormente nello spazio sottoretinico, fino a formare una struttura nota come membrana neovascolare coroideale (CNV), da cui si ha una fuoriuscita di fluidi e sangue che si accumulano sotto la macula. L’accumulo di liquidi in questo punto compromette seriamente e rapidamente la struttura anatomica e la funzionalità maculare, che essendo rimossa dalla sua posizione fisiologica, viene separata dalla sua fonte di ossigeno e nutrimento. La mancanza prolungata di ossigeno e nutrienti causa la morte delle cellule della macula e conseguente perdita della visione centrale. La perdita della visione centrale può instaurarsi anche a causa della formazione di tessuto cicatriziale sulla macula.
4 Tipologie di maculopatia essudativa
- Tipo 1 o CNV occulta: si sviluppa al di sotto dell’epitelio pigmentato retinico RPE. Viene diagnostica solo grazie all’angiografia con verde indocianina ed alcune volte nelle forme più gravi si presenta con emorragie retiniche. Il paziente percepisce un’immagine intera, ma con distorsioni.
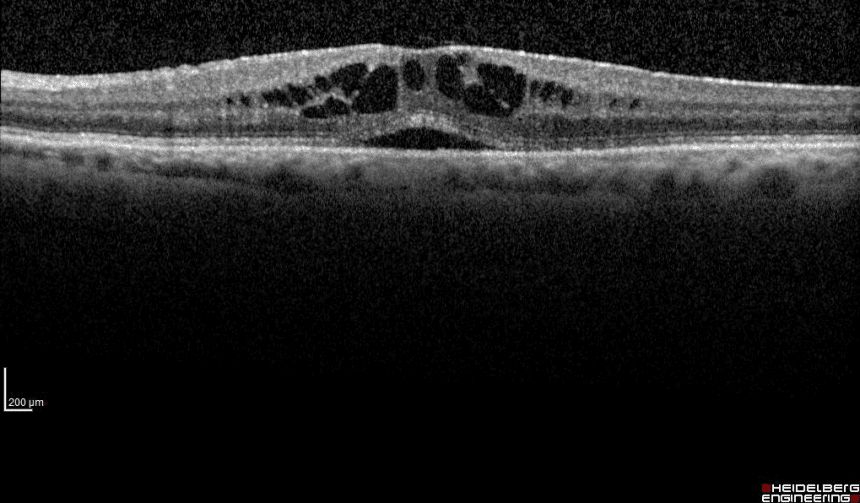
- Tipo 2 o CNV classica: si sviluppa al di sopra dell’epitelio pigmentato retinico EPR. Può essere diagnosticata sia con la Tomografia a Coerenza Ottica (OCT) ad alta definizione o sia con l’Angiografia a Fluorescenza (FAG) o con il Verde Indocianina (ICGA); solitamente questa è la forma più grave perché sviluppa grandi cicatrici a causa delle quali si perde la visione centrale.
- Tipo 3 o vasculopatia polipoidale (IPVC): si sviluppa al di sotto dell’epitelio pigmentato retinico, ma ha una forma pseudopoidale circoscritta e ben definita.
- Tipo 4 o proliferazione retinica angiomatosa (RAP): si sviluppa all’interno della retina e prolifera verso il basso creando una anastomosi, cioè una patologica comunicazione direttamente tra arteria retinica ed una vena della coriocapillare. Solitamente sono le forme che meglio rispondono alla terapia intravitreale con anti-VEGF.
Sintomi
I pazienti affetti dalla maculopatia essudativa percepiscono sintomi quali distorsione delle immagini, percezione ondulata delle linee, presenza di uno scotoma al centro della visione che possono instaurarsi repentinamente e diventare subito molto gravi. L’evoluzione della patologia può diventare estremamente rapida e drammatica in presenza di emorragia a livello della membrana vascolare: in questi casi la perdita della visione centrale può avvenire anche in pochi secondi.
Per i motivi sopraesposti sopra, diventa evidente che la prevenzione della maculopatia essudativa è di fondamentale importanza per evitare o quantomeno limitare i danni derivanti da questa grave patologia oculare. La prevenzione è importante per tutte le persone di età superiore ai 50 anni ed è fondamentale per i pazienti affetti da AMD atrofica, nei quali il rischio di evoluzione in AMD essudativa è sempre presente.
Diagnosi
Trattamento
Il trattamento per l’AMD essudativa prevede una serie di iniezioni intravitreali a base di farmaci anti-VEGF. Anche se questa procedura è efficace nell’impedire o ritardare la perdita della visione centrale, è bene tener presente che ad oggi non esiste alcun trattamento definitivo per l’AMD essudativa e pertanto la prevenzione rappresenta un’arma particolarmente efficace per difendersi da questa grave patologia retinica.
Il processo infiammatorio che causa l’insorgenza dell’AMD essudativa coinvolge una serie di reazioni biochimiche note come cascata del complemento; questa può essere modulata grazie a un fattore denominato fattore CFH. Il fattore CFH regola l’entità della risposta infiammatoria, che nelle persone sane aumenta o diminuisce a seconda delle necessità; alcune varianti del gene che codifica per il fattore CFH sono correlate all’incapacità del fattore CFH di modulare – in particolare di “frenare” e tenere sotto controllo – la risposta infiammatoria, pertanto nei soggetti in cui vi è la presenza di una di queste varianti genetiche del fattore CFH, esiste un maggiore rischio d’insorgenza dell’AMD (suscettibilità genetica).
Dal momento che le varianti individuate del gene CFH responsabili della suscettibilità genetica per l’AMD sono diverse, sono disponibili diversi test genetici che permettono di evidenziarne la presenza. Il test è consigliato soprattutto alle persone che hanno una familiarità per l’AMD essudativa, ma anche di tipo atrofico. Presentare suscettibilità genetica per l’AMD non significa essere destinati ad ammalarsi, ma al contrario, questa informazione permette di adottare protocolli di prevenzione in grado di ridurre il rischio d’insorgenza di questa patologia. I protocolli di prevenzione si basano sull’adozione di stili di vita molto sani, che escludano il più possibile la presenza di fattori di rischio ambientali e comportamentali. Perché possano essere di aiuto, i test genetici devono essere rigorosamente eseguiti e interpretati da genetisti esperti.
Patologia e trattamento in video
Hai bisogno di altre informazioni?
Non esitare a contattarmi per qualsiasi dubbio o chiarimento. Valuterò la tua problematica e sarà premura mia e del mio staff risponderti il più velocemente possibile.