Resultados promissores na fase três do estudo de terapia genética LHON
A neuropatia óptica hereditária de Leber (LHON) é uma doença neurodegenerativa mitocondrial do nervo óptico herdada da mãe.
É a doença do DNA mitocondrial (mtDNA) mais comum, afetando cerca de 1 em 30.000 a 1 em 50.000 pessoas, principalmente adultos jovens do sexo masculino. A fisiopatologia da LHON é caracterizada pela perda seletiva de células ganglionares da retina (RGCs) e seus axônios, levando à perda progressiva e rápida da visão bilateral. O prognóstico visual é ruim e a maioria dos pacientes apresenta deficiência visual de 20/200 no primeiro ano de início da doença.
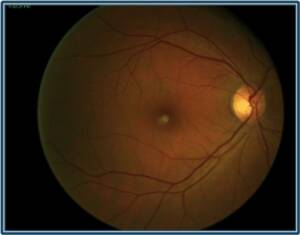
Neuropatia óptica hereditária de Leber
Ouça a patologia Andrea Cusumano Neuropatia Óptica Hereditária de Leber https://andreacusumano.com/wp-content/uploads/2025/05/neuropathyotticaleber.mp3 Index A Neuropatia Óptica Hereditária de Leber (LHON) é uma doença mitocondrial muito comum.
O REVERSE é um ensaio clínico randomizado, duplo-cego e multicêntrico de Fase 3 que avalia a eficácia de uma única injeção intravítrea de rAAV2/2-ND4 em indivíduos com perda de visão por neuropatia óptica hereditária de Leber (LHON).
O rAAV2/2-ND4 (GS010) é um vírus adeno-associado com defeito de replicação recombinante, sorotipo 2, que contém um cDNA modificado que codifica a proteína ND4 mitocondrial humana selvagem e uma proteína MTS específica de translocação na matriz mitocondrial.
Um total de 37 indivíduos portadores da mutação m.11778G>A (MT-ND4) e com duração da perda de visão variando de 6 a 12 meses foram tratados. O olho direito de cada sujeito foi designado aleatoriamente para receber rAAV2/2-ND4 (GS010) ou injeção de placebo. O olho esquerdo recebeu tratamento não atribuído ao olho direito.
Inesperadamente, melhora visual sustentada foi observada em ambos os olhos durante o período de acompanhamento de 96 semanas. Ao final do período, os olhos tratados com rAAV2/2-ND4 mostraram uma melhora média na acuidade visual corrigida (BCVA) de -0,308 LogMAR (+15 letras ETDRS). Uma melhora média de -0,259 LogMAR (+13 letras ETDRS) foi observada nos olhos tratados com placebo.
Na semana 96, 25 indivíduos (68%) tiveram recuperação clinicamente relevante de BCVA desde a linha de base em pelo menos um olho e 29 indivíduos (78%) tiveram melhora da visão em ambos os olhos.
Supõe-se que os efeitos positivos produzidos pelo tratamento, também no olho contralateral, sejam atribuíveis à transferência interocular do vetor viral rAAV2 / 2-ND4.
Em um estudo com roedores, um corante marcador injetado intravítreo em olhos de ratos detectou nervos ópticos dos olhos não injetados contralaterais: isso sugere que há uma transferência axonal ou glial através das vias visuais anteriores. Também há evidências para apoiar a disseminação transneuronal, possivelmente por meio de mecanismos de transferência sináptica.
Foi demonstrado que as mitocôndrias podem migrar longas distâncias nos axônios para distribuir energia e permitir a atividade neuronal distal; de fato, as mitocôndrias dentro dos axônios RGC também podem ser engolfadas em vesículas e exportadas para astrócitos que estão em alta densidade na cabeça do nervo óptico e depois armazenadas em os endossomos.
A densa rede de processos astrocíticos interconectados poderia, portanto, permitir a transferência de longa distância célula a célula de elementos citoplasmáticos por meio de junções de membrana. Outro mecanismo hipotético subjacente à melhora contralateral é a plasticidade cerebral com reorganização das áreas visuais contribuindo para a melhora visual dos olhos contralaterais não injetados.
A terapia visa salvar as células ganglionares da retina da mutação causada pela LHON, substituindo o gene defeituoso.
Este importante passo soma-se às terapias gênicas recentemente introduzidas no tratamento de outras patologias retinianas hereditárias-familiares graves e incapacitantes.
Nota ao leitor:
Quando um estudo está na fase três: chegou ao ponto de entender a eficácia do medicamento, se traz mais benefícios do que os similares já existentes no mercado e qual a relação entre risco e benefício. Nesta fase, para validar a eficácia do estudo, centenas ou milhares de pacientes são "inscritos".

